| Startseite |
Die MO's sind im Rahmen des Hartree-Fock-Modells definiert:
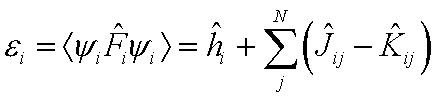
wobei
ei
die MO-Energien sind, yi
die MO's. In diesen MO's ist also die Elektronen-Elektronen-Wechsel-
wirkung in gewisser Weise berücksichtigt, s. SCF (Die
Gesamt-Energie ist aber nicht die Summe dieser MO-Energien!).
Im Output erscheinen diese Orbitale in folgender Weise: Hier am Beispiel O2 (STO-6G)
------------------
MOLECULAR ORBITALS
------------------
1 2
3 4
5
-20.6790
-20.6789 -1.5051 -1.0215 -0.5686
A1G A2U
A1G A2U A1G
1 O 1 S 0.705204 0.704809 -0.161156 -0.177040
0.057267
2 O 1 S 0.007394 0.011071 0.593189 0.775892
-0.302074
3 O 1 X 0.000000 0.000000 0.000000 0.000000
0.000000
4 O 1 Y 0.000000 0.000000 0.000000 0.000000
0.000000
5 O 1 Z 0.000236 0.003270 0.153580 -0.142310
0.619262
6 O 2 S 0.705204 -0.704809 -0.161156 0.177040
0.057267
7 O 2 S 0.007394 -0.011071 0.593189 -0.775892 -0.302074
8 O 2 X 0.000000 0.000000 0.000000 0.000000
0.000000
9 O 2 Y 0.000000 0.000000 0.000000 0.000000
0.000000
10 O 2 Z -0.000236 0.003270 -0.153580 -0.142310 -0.619262
6 7
8 9
10
-0.5525
-0.5525 -0.0997 -0.0997 0.6134
EU EU
EG EG
A2U
1 O 1 S 0.000000 0.000000 0.000000 0.000000
-0.079386
2 O 1 S 0.000000 0.000000 0.000000 0.000000
0.493958
3 O 1 X 0.665566 0.000000 0.757543 0.000000
0.000000
4 O 1 Y 0.000000 0.665566 0.000000 0.757543
0.000000
5 O 1 Z 0.000000 0.000000 0.000000 0.000000
0.908740
6 O 2 S 0.000000 0.000000 0.000000 0.000000
0.079386
7 O 2 S 0.000000 0.000000 0.000000 0.000000
-0.493958
8 O 2 X 0.665566 0.000000 -0.757543 0.000000
0.000000
9 O 2 Y 0.000000 0.665566 0.000000 -0.757543
0.000000
10 O 2 Z 0.000000 0.000000 0.000000 0.000000
0.908740
In der obersten Zeile steht die Nummer des MO's (das
niedrigste hat die Nummer 1). In der nächsten Zeile steht die MO-Energie (in eV!).
3. Zeile: Symmetrie (diese richtet sich nach der Symmetrie-Angabe im $DATA-Block;
hier D2h). 4. Zeile: fortlaufende Zahl der Basisfunktion, Atomsymbol, Art der
Basisfunktion - hier s-Typ, der folgende Zahlenwert gibt das Gewicht des AO's in
der Linearkombination zum MO an.
MO1 hat also eine Energie von -20.6790 eV, A1g-Symmetrie und besteht
aus einer Linearkombination der beiden s-AO's und des pz-AO's an den
beiden O-Atomen. Mehr Details: O2-Output
Instruktiv ist die Betrachtung einer linearen Kette von H-Atomen, da man dabei die Abhängigkeit vom Basissatz, den Zusammenhang mit Knotenebenen und die Beziehung zum Hückelmodell gut sehen kann. Bei cyclischen Systemen ist der Zusammenhang Orbitalenergie - Anzahl der Knotenebenen undurchsichtiger (s. cycl. H5).
Eine wichtige Frage ist, welche Bedeutung den Orbitalen zukommt, wenn ein Mehrelektronensystem vorliegt (s. Slater-Determinante) und wenn Korrelationseffekte berücksichtigt werden. Da die Orbitale Ein-Elektronen-Wellenfunktionen sind, könnte man annehmen, dass die Elektronenanzahl keine Rolle spielt, d. h. dass die MO's von linearen H43+ (Ein-Elektronensystem) und H42+ (Zwei-Elektronensystem) identisch sein sollten (das ist nicht der Fall!). Was passiert bei Post-Hartree-Fock-Methoden (CI, MCSCF)?
| Seitenanfang |